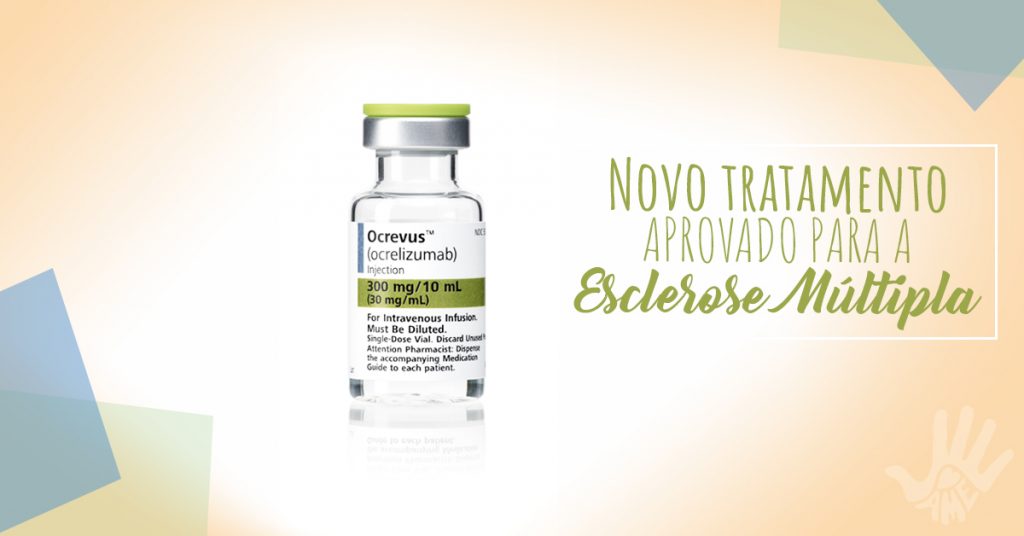
Esta semana a Anvisa aprovou um medicamento inédito para tratar as formas EMRR e EMPP de esclerose múltipla, o Ocrevus.
O que é e como funciona?
Ocrelizumabe (Ocrevus) é um anticorpo monoclonal, um tipo de fármaco desenvolvido para atacar alvos específicos no sistema imunológico. Ocrelizumab foi projetado para direcionar um marcador (CD20) na superfície das células B, um tipo de glóbulo branco (linfócito) que é pensado para influenciar a resposta imune anormal que ataca a mielina que envolve as células nervosas. As células B direcionadas são destruídas.
Como é tomado Ocrelizumab?
Ocrelizumab é tomado como uma infusão intravenosa (gotejamento). A primeira dose é administrada como duas infusões separadas. Outras doses são administradas como uma infusão a cada seis meses.
Pesquisas Ocrelizumabe
Em 2015, os primeiros estudos mostraram que o Ocrevuz poderia retardar pelo menos 12 semanas na progressão da esclerose múltipla primária progressiva em seus estágios iniciais, como anunciou o Hospital Vall d’Hebron, em Barcelona, que liderou o desenvolvimento do estudo. Até agora, não havia tratamento para este tipo de esclerose múltipla, mas o estudo desta droga abre a possibilidade de termos um primeiro tratamento para estes pacientes, até o início de 2016 os resultados serão submetidos às autoridades reguladoras para aprovação do novo medicamento.
Quais são os resultados até agora?
EMRR
Em uma fase II, 24 semanas, ensaio clínico, 218 pessoas foram divididas em grupos que receberam uma das duas doses de Ocrelizumab (600mg e 2000mg), interferon beta-1a (Avonex) ou placebo. Após 24 semanas, o número de lesões ativas medida por exames de ressonância magnética foi 89% menor no grupo de dose baixa e 96% menor no grupo de dose elevada em comparação com o grupo placebo.
Às 24 semanas, a taxa de recaída anual foi de 0,13 no grupo de dose baixa e de 0,17 no grupo de dose elevada em comparação com 0,36 para pessoas com interferon beta e 0,64 no grupo placebo.
Opera I e II – ocrelizumab em comparação com o interferão beta 1a (Rebif)
Esses estudos de fase III recrutaram 1656 participantes com EM remitente-recorrente que tomaram Oucrelizumab 600mg a cada 6 meses ou interferon beta 1a (Rebif) três vezes por semana durante aproximadamente dois anos.
Ao longo dos dois anos dos ensaios clínicos, o Ocrelizumab reduziu o número de recidivas em 50% em relação ao interferon beta 1a, diminuiu a progressão da incapacidade sustentada durante 3 e 6 meses e reduziu significativamente o número de lesões observadas em exames de RM em comparação com o interferon beta. A perda de volume do cérebro foi reduzida e o número de participantes sem evidência de progressão da doença (NEDA) foi aumentado nos grupos de tratamento de Ocrelizumab em comparação com o interferon beta 1a.
EMPP
Oratório – ocrelizumab em comparação com o placebo
Este estudo de fase III recrutou 732 participantes com EM Primária-progressiva e EDSS de 3 a 6,5 que tomaram 600 mg de Ocrelizumab ou placebo por infusão a cada 6 meses por mais de 2 anos.
A principal medida do estudo foi o início da progressão da deficiência. Isso foi medido pelo número de participantes com um EDSS aumentado que ainda era evidente 3 meses depois. O estudo também registrou o número de participantes com um EDSS aumentado ainda evidente após 6 meses, velocidade de caminhada acima de 25 pés e volume de lesões cerebrais.
Menos pessoas que tomaram Ocrelizumab tiveram um aumento na incapacidade, em comparação com o placebo. Um aumento na incapacidade que durou 3 meses foi observado em 32,9% daqueles que tomaram Ocrelizumab e 39,3% dos que receberam placebo. Além disso, o aumento da incapacidade que durou pelo menos 6 meses foi observado em 29,6% tomando Ocrelizumab e 35,7% tomando placebo. Comparando os dois grupos, as pessoas que tomaram Ocrelizumab foram 24% menos propensas a ter um aumento na sua incapacidade do que aqueles que tomaram placebo.
Após 120 semanas de tratamento, a velocidade de caminhada de mais de 25 pés foi 39% mais lenta para Ocrelizumab, em comparação com 55% mais lento para o placebo. O volume de lesão cerebral diminuiu 3,4% com Ocrelizumab e aumentou 7,4% com placebo. A perda de volume cerebral foi de 0,9% para Ocrelizumab e 1,09% para o placebo.
Acompanhe as pesquisas completas nessa matéria em nosso site: http://bit.ly/2F9vxgc
O Ocrevus ainda não consta na lista de tratamentos fornecidos pelo SUS no Brasil, mas é mais uma alternativa de tratamento para as pessoas com esclerose múltipla remitente-recorrente e esclerose múltipla primária-progressiva no país. Assim como os outros medicamentos, Ocrevus não cura a EM, mas ajuda no controle do avanço da doença.
Fontes:
http://bit.ly/2CTdogT